Dr. José Ramón Gómez Mancebo
El pasado 4 de diciembre de 2006 se dio a la comunidad el resultado preliminar del estudio ILLUSTRATE, ensayo clínico en el cual se comparaban los efectos de un nuevo medicamento inhibidor de la proteína de transferencia de ésteres de colesterol (CETP), conocido farmacológicamente como torcetrapib asociado a la atorvastatina, una estatina con un ya largo historial clínico de efectos beneficiosos, ambos comparados contra el efecto aislado de la atorvastatina. Los datos indicaron que el grupo de pacientes tratado con la combinación torcetrapib-atorvastatina acumularon más muertes y eventos cardiovasculares. Fuera del efecto económico impactante sobre la compañía productora de ambos medicamentos: Pfizer, que para el momento había invertido mil millones de dólares, lo cual junto con la caida de sus acciones en la bolsa, fue el principal motivo de que la noticia permeara a los medios comunicacionales generales, decidió detener todo el programa de desarrollo del medicamento. Esta parte de la noticia es la que más afecta a la intensa búsqueda de la prevención y tratamiento de la enfermedad coronaria. La noticia implica que una de las mayores esperanzas en elevar el colesterol HDL, conocido como “bueno” pierda toda opción de aplicación clínica. El investigador principal del estudio ILUSTRATE, el Dr. Steven Nissen, de la Cleveland Clinic, Ohio, indicó que se trataba de un ensayo multicéntrico, aleatorizado, en el cual a 1200 personas conocidas enfermas coronarias, se les realizaba ultrasonido intracoronario. Ya en Chicago, en noviembre pasado, en la reunión de la American Heart Association, habíamos escuchado del propio Dr. Nissen, la gran esperanza que se depositaba en los resultados de este estudio, así que hasta para él fue una desagradable sorpresa la información emitida por el comité de seguridad del ensayo: 82 pacientes que tomaban la combinación torcetrapib y atorvastatina murieron, comparados con los 51 pacientes muertos en el brazo de atorvastatina sola.
Ya se había publicado previamente el efecto de aumento de la presión arterial producido por el torcetrapib entre 2 y 4 mm Hg, lo cual aunque parece mínimo, significa en proyección a la población, un aumento del 20% de mortalidad por accidente vascular cerebral (ACV) y de un 12% de mortalidad por enfermedad isquémica cardíaca (1).
No se conoce con certeza, para este momento, la causa de este aumento de mortalidad en el grupo tratado con torcetrapib-atorvastatina, teóricamente podría achacársele al efecto de elevación de los valores de presión arterial, sin embargo, el protocolo permitía el control de tales cambios con la adición de antihipertensivos; otra posibilidad, es la relativamente nueva diferencia entre las moléculas de HDL-C. El planteamiento es que el HDL-C producido por la inhibición de CETP ya es “maduro” y podría ser anormal y en lugar de descargar o “limpiar” de LDL-C (colesterol malo) las paredes vasculares, como ocurre con el HDL-C conducido por la apoA-1, y llevarlo al hígado, tendría un efecto proaterogénico y no antiaterosclerótico (gráfico 1).
 Gráfico 1
Gráfico 1
¿POR QUÉ ELEVAR EL COLESTEROL HDL?
Los grandes ensayos clínicos, que evaluaron la disminución del colesterol LDL, demostraron que cuanto más bajo fuese daba mejores resultados en el control de la morbilidad y la mortalidad de los pacientes con enfermedad vascular aterosclerótica. El estudio REVERSAL demostró detención de la progresión de la aterosclerosis pero no se llegó hasta la regresión (2). Los niveles obtenidos hasta bajar de 70 mg/dl fueron el resultado de la elevación de las dosis de estatinas, lo cual ha conducido hasta una reducción del 35% de los eventos cardiovasculares, pero aún queda un porcentaje muy importante de personas en riesgo de enfermedad, por lo cual el próximo enfoque fue el de elevar el colesterol HDL, que para el momento había sido relegado a un segundo plano. El control
de varios factores de riesgo simultáneos debe ser muy seriamente tomado en cuenta, sobre todo porque se avecina un incremento de la incidencia de enfermedad vascular en los próximos 15 años, a consecuencia de las actuales epidemias de obesidad y diabetes, realimentadas entre sí. Hay que eliminar el tabaquismo, controlar la dieta e incentivar el ejercicio para controlar el auge de la obesidad, regular y controlar con fuerza la hipertensión, mantener los niveles de control de LDL-C pero insistir también en la elevación del HDL-C. El promedio de HDL como valor mínimo aceptado actualmente es de 45 mg/dl para el hombre y de 55 mg/dl para la mujer. Niveles superiores a 60 mg/dl se consideran buenos y existe una relación de que por cada 1 mg/dl de incremento de HDL-C hay una reducción entre el 2 % y el 3% de la incidencia de enfermedad coronaria.
FUNCIONES DEL COLESTEROL HDL
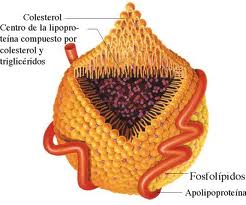
Los beneficios del HDL-C parecen deberse al transporte reverso del colesterol desde las paredes arteriales hacia el hígado, donde se prepara su excreción. Pero además, se han descubierto propiedades anti-inflamatorias, antioxidantes, antitrombóticas e inductoras de óxido nítrico. La presencia de estas propiedades no han podido demostrar beneficios in vivo en grandes poblaciones, a las cuales se les pudiera elevar el HDL-C. De las pocas situaciones clínicas evaluadas, una de las más prometedoras es la del ApoA-1 Milano. Esta es una variante poco usual del principal constituyente del HDL-C, fue descubierta por los Dres. Cesare Sirtori y Guido Francheschini, de la Universidad de Milan, en Italia, en un grupo de italianos, parientes entre sí, con valores de HDL-C bajos pero sin enfermedad cardiovascular (3). Posteriormente el Dr. Prediman Shah, en Los Angeles, indujo regresión de la aterosclerosis en modelos animales después de inyectar ApoA-1 Milano (4). Más recientemente el Dr. Nissen, realizó la aplicación en humanos, como describiré más adelante.
¿COMO SUBIR EL COLESTEROL HDL?
Hay demostración de elevación del HDL-C mediante cambios en el estilo de vida como realizar ejercicio regularmente, dejar de fumar, perder peso y hacer dieta adecuada, e incluso beber alcohol moderadamente. La elevación de HDL-C a través de estos efectos no farmacológicos es modesta. A continuación, a manera de gráficos coloco en forma esquemática los efectos mencionados sobre el HDL (gráficos 2 al 8)





 Existen algunas drogas en el mercado, que elevan el HDL-C. La niacina, no disponible en Venezuela, en dosis de 2000 mg puede elevar hasta 30% el HDL-C. Su principal efecto colateral es el rubor, pero también produce intolerancia a los carbohidratos, elevación del ácido úrico y anormalidades de la función hepática.
Existen algunas drogas en el mercado, que elevan el HDL-C. La niacina, no disponible en Venezuela, en dosis de 2000 mg puede elevar hasta 30% el HDL-C. Su principal efecto colateral es el rubor, pero también produce intolerancia a los carbohidratos, elevación del ácido úrico y anormalidades de la función hepática.
Los fibratos, disponibles en Venezuela el gemfibrozil, el bezafibrato y el ciprofibrato, no tenemos fenofibrato. También tienen un modesto efecto elevador del HDL-C.
Las glitazonas, agonistas PPARs, que detallaré adelante. En Venezuela están disponibles la rosiglitazona y la pioglitazona.
Hay actualmente drogas en desarrollo.
Inhibidores de CETP. De este grupo ya mencionamos el dramático final del torcetrapib, pero no sabemos que sucederá con otro similar conocido por sus siglas JJT-705, perteneciente a Japan Tobacco/Roche, que estaba por iniciar estudios de Fase 3. El Dr. Michael Millar de la Universidad del Centro Médico de Maryland, demostró en ensayos fase 2, que el compuesto JT eleva el HDL alrededor de 35% a 40%, algo menos de lo que era capaz el torcetrapib. Existía incertidumbre, y hoy todavía más, en relación a los inhibidores de CETP, incluso en algunos modelos animales se habían demostrado resultados conflictivos con indicadores de empeoramiento. Teóricamente estos bloqueado-
res impiden la transferencia del colesterol del HDL al LDL. Si simultáneamente se agregan estatinas, y se disminuye el LDL-C también se bloquea la transferencia de colesterol al LDL y se podría bloquear la transferencia de ese colesterol al hígado. Es posible que esta sea la causa de un resultado obtenido en roedores en el cual hubo un aumento de aterosclerosis.
La vacuna de CETP. La compañía Avant Pharmaceuticals ha desarrollado una vacuna contra el CETP, que ha demostrado elevar el HDL-C en modelos animales de aterosclerosis. Los ensayos clínicos preliminares indican un incremento modesto del 8%, no producido en pacientes que toman estatinas, así que la indicación, si llega a darse, será en pacientes con HDL-C bajo con LDL-C normal. Por supuesto que la atención sobre esta vacuna se eleva ante el riesgo que sería bloquear el CETP, si esta acción no fuese benéfica y se produjese un daño irreversible al recibir un anticuerpo contra el transportador.
Así que hasta ahora se ha trabajado con el concepto mecanístico del bloqueo CETP, pero la comunidad científica está descubriendo la adversidad que significa que aún hay pasos intermedios o resultados posteriores a la transferencia del colesterol LDL-C que no responden a la causa-efecto.
Los agonistas de PPARs son otra clase de drogas ya en uso y en desarrollo que elevan el HDL-C mediante su efecto positivo sobre los receptores activados de proliferación de peroxisomas (PPAR). Los PPARs son receptores nucleares que activan un gen, el ABC-A1, que a su vez estimula el primer paso del transporte reverso de colesterol fuera de las células hacia las partículas de HDL-C (gráfico 1). Hay tres tipos de PPARs alfa, gamma y delta. Todos son objetivos para actuar como drogas. Los fibratos se unen al PPAR alfa, y producen, como se dijo, aumento del HDL-C pero también disminución de los triglicéridos. Los PPAR gamma elevan el HDL modestamente, y su efecto más importante es la reducción de la resistencia a la insulina. Las glitazonas utilizadas en la diabetes mellitus actúan como agonistas de PPAR gamma. Los PPAR delta parecen tener los tres efectos (tabla 1).

HDL mimético. De todas las aproximaciones para elevar HDL, la más obvia es administrar HDL o su constituyente principal el ApoA-1, o agentes que mimeticen estas substancias. Esta es la base de los estudios sobre el ApoA-1 Milano mediante el ETC-216 de Esperion que es un ApoA-1 Milano mimético sintético. Esta molécula tiene varias limitaciones: por ser muy grande no está disponible para su uso oral, solo por vía intravenosa, de manera que no puede ser utilizada en tratamientos crónicos, es muy cara y aparentemente muy laboriosa su confección.
Péptidos orales. Para 2004, Esperion desarrollaba péptidos activos por vía oral. El portafolio de Esperion para el transporte reverso de colesterol lo componían:
ETC-216, ya mencionado, que es la versión recombinante de ApoA-1 Milano
ETC-588, también de administración intravenosa, descrito como la esponja de colesterol, compuesto por un fosfolípido liposoma que acepta colesterol desde el HDL y los tejidos periféricos. Se estudia en ensayos de aterosclerosis carotídea.
ETC-642, complejo péptido/fosfolípido que mimetiza el HDL y promueve el transporte reverso de colesterol.
ESP 31015, molécula pequeña oral, disminuye el LDL y eleva el HDL, inhibe la progresión de aterosclerosis en estudios animales.
La compañía Pfizer adquirió Esperion ante el gran potencial de la ApoA-1 Milano y sus miméticos. Novartis/Bruin Pharmaceuticals de Los Angeles, tiene un péptido en desarrollo identificado como D4F, y han demostrado disminución de aterosclerosis en ratones, en tratamiento oral.
Receptor SR-BI. Otra posible, pero controversial aproximación de la manipulación del HDL es aumentar la regulación del receptor SR-B1 en el hígado (gráfico 1). El receptor SR-BI limpia el HDL del plasma mediante el tránsito de colesterol desde la sangre a la bilis, esto produce una disminución de HDL, pero el punto importante parece ser no elevar el HDL, sino permitir que trabaje mejor, por ejemplo, se ha observado en modelos murinos que la ausencia de SR-BI produce un aumento de HDL pero un concomitante aumento de aterosclerosis. La lógica parece ser que si el hígado “succiona” el HDL de la sangre, a través del aumento de los receptores SR-BI, se incrementaría el flujo de colesterol desde las paredes arteriales con un nivel bajo de HDL plasmático. Este planteamiento va en contra de la actual intención de elevar el HDL-C, sin embargo, coincide con las familias a las cuales se les describió el ApoA-1 Milano, que estando protegidas contra aterosclerosis, tenían un bajo nivel de HDL-C (3)
ESTADO ACTUAL DE LA INVESTIGACIÓN SOBRE LA ELEVACIÓN DEL HDL-C
En mayo 2006, se inició por la Universidad de Oxford, un nuevo ensayo clínico para evaluar la elevación de colesterol HDL y su capacidad de protección contra los eventos cardiovasculares. El estudio se conoce como Heart Protection Study 2 Treatment of HDL to Reduce the Incidente of Vascular Events (HPS 2-THRIVE), evaluará la nueva combinación de niacina de liberación prolongada y un bloqueador de prostaglandina D2 para evitar el rubor. El punto final primario combinado incluye la aparición de infarto miocárdico, ACV o revascularización miocárdica, en pacientes con enfermedad vascular conocida. Se pretende enrolar 20.000 pacientes. El tratamiento estima elevar el HDL-C en 20% lo cual podría proyectar una reducción del 20% del riesgo del punto final primario combinado. Los investigadores de este estudio planean reclutar pacientes entre 50 y 80 años con historia de infarto, ACV o enfermedad arterial periférica; aproximadamente 7000 tendrán diabetes mellitus tipo 2. Los niveles de LDL-C de los pacientes serán optimizados con estatinas antes de la aleatorización hacia placebo o la droga elevadora de HDL-C. Cada paciente será seguido por 4 años.
Ha habido dos grandes problemas con el HDL-C. Primero se sabe que la población con HDL-C elevado tienen mucha menos incidencia de enfermedad coronaria, lo que no se sabe hasta ahora con claridad es si la elevación de HDL-C mediante fármacos es benéfica, incluso en los estudios en los que la utilización de fibratos elevaron modestamente los niveles de HDL-C los resultados han sido confusos. Para el año 2001 se publicó el estudio HATS (HDL Atherosclerosis Treatment Study) que evidenció el beneficio de combinar un tratamiento con estatina y niacina. El ensayo de 3 años de seguimiento, placebo controlado indicó que la sinvastatina más la niacina, con dosis promedio diarias de 13 mg y 2,4 g, respectivamente, detuvieron la progresión angiográfica de la aterosclerosis y redujeron los eventos clínicos mayores (5).
Resultados de otro estudio, el ARBITER-2 (Arterial Biology for the Investigation of the Treatment Effects of Reducing Colesterol), demostraron que la adición de niacina de liberación prolongada al tratamiento con estatina puede disminuir la progresión de la aterosclerosis, medida a través del grosor íntima-media, en pacientes con enfermedad arterial coronaria con HDL-C bajo (6)
Los fibratos, específicamente el genfibrozil, demostró por primera vez en 1999, que la elevación de HDL-C y la disminución de los triglicéridos redujeron los eventos cardiovasculares mayores, incluso sin disminuir el LDL-C. Estos resultados provienen del estudio VA-HIT (Veteran Affaire High-Density Lipoprotein Cholesterol Intervention Trial) (7).
Sin embargo, la información más impactante sobre la elevación del HDL-C fue la publicada también por el Dr. Steven Nissen, en solo 47 personas a las cuales se les infundió una substancia recombinante de Apo A-1 Milano y produjo una regresión significativa de la aterosclerosis coronaria (8).
Están en planes otros estudios como el AIM-HIGH (Atherothrombosis Intervention in Metabolic Syndrome with Low HDL Colesterol/High Triglyceride and Impact on Global Health Outcomes), patrocinado por el NIH (Nacional Institutes of Health) con la intención de evaluar simultáneamente la disminución de LDL-C y la elevación de HDL-C, mediante el tratamiento con niacina de liberación prolongada más sinvastatina o sinvastatina sola. Otro estudio en camino es el ACCORD que evalúa el fenofibrato más estatina vs estatina sola en pacientes con diabetes mellitas tipo 2.
La elevación del HDL-C parece una estrategia buena, pero quedan problemas a ser aclarados. Se conocen diferentes tipos de HDL y aparentemente, la cualidad podría ser tan importante como la cantidad. Por ejemplo las partículas de HDL-C enriquecidas con ApoA-1 son buenas, pero las enriquecidas con ApoA-2 no. Como ya se comentó previamente los individuos con ApoA-1 Milano cualitativamente bueno, cuantitativamente tenían un HDL-C bajo, por otro lado las mutaciones de CETP producen elevación del HDL-C pero de características disfuncionales que aparentemente no son protectoras (9). Recordemos que el LDL-C tiene un comportamiento parecido. Cuando es pequeño y denso, el LDL-C es más dañino que cuando no lo es. De todas maneras, el HDL-C parece más complicado, solo por sus vías metabólicas descritas, nueve hasta ahora, se diferencia del LDL-C que tiene dos receptores relacionados con su captación y degradación.
En mayo pasado, el Dr. Fumihiko Matsuura publicó (10) el efecto del bloqueo CETP y la formación del HDL-C para evaluar su funcionalidad para revertir el transporte de colesterol. El HDL-C formado posterior al bloqueo de CETP es predominantemente HDL-2, más grande que la molécula regular que domina en los individuos normales, hasta este estudio clínico se desconocía si este tipo de HDL-C puede extraer el colesterol vascular. Este estudio comparó el HDL-C de individuos normales y de otros con deficiencia de CETP. El resultado fue que el HDL-C resultante del grupo con CETP deficiente tuvo entre 2 y 3 veces más efectividad en el transporte reverso del colesterol. Los autores reportan que la deficiencia de CETP, inclinan la función del HDL hacia el mayor contenido de LCAT (lecitin colesterol acyltransferasa) y apolipoproteina E (Apo E), que conduce el eflujo de colesterol por esterificación en las partículas de HDL. El HDL formado por la inhibición del CETP está cargado de colesterol y según estos resultados parece que la Apo E permite a la partícula de HDL2 expandirse y aceptar más colesterol (11). Además, el eflujo de colesterol desde las células espumosas hasta el HDL2 es desviado en mayor proporción a la mediación de un transportador conocido como ABCG1, presente en los macrófagos.
Estos resultados variables indican que es probable que la inhibición del CETP sea más exitosa en grupos específicos de pacientes y no como una estrategia general.
Estamos lejos de saber todo sobre el metabolismo lipídico pues aun no conocemos los mecanismos intrínsecos que utiliza el HDL-C para sus beneficios. Sabemos que es protector, pero no sabemos cómo, y parece depender de su concentración, pero no siempre.
El torcetrapib y su corta historia nos indica que en investigación no todo lo que brilla es oro, y muchas veces las estrategias terapéuticas deben ser enfocadas a situaciones específicas, de grupos de pacientes específicos.
REFERENCIAS:
1. Lewington S, Clarke R, Qizilbash N, et al. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002; 360:1903-1913
2. Nissen SE, Tuzcu EM, Schoenhagen P, Brown BG, et al. Effect of intensive compared with moderate lipid-lowering therapy on progression of coronary atherosclerosis: a randomized controlled trial. J Am Med Ass 2004;291:1071-80
3. Franceschini G, Sirtori CR, Capurso A 2nd, Weisgraber KH, Mahley RW. A-I Milano apoprotein. Decreased high density lipoprotein cholesterol levels with significant lipoprotein modifications and without clinical atherosclerosis in an Italian family. J Clin Invest 1980; 66:892-900
4. Shah PK, Nilsson J, Kaul S, Fishbein MC, et al. Effects of recombinant ApoA-1 (Milano) on aortic atherosclerosis in apolipoprotein E-deficient mice. Circulation 1998;97:780-785
5.Brown BG, Zhao XQ, Chait A, et al. Simvastatin and niacin, antioxidant vitamins, or the combination for the prevention of coronary disease. N Engl J Med 2001; 345:1583-1592.
6.Taylor AJ, Sullenberger LE, Lee HJ, et al. Arterial Biology for the Investigation of the Treatment Effects of Reducing Cholesterol (ARBITER) 2: A double-blind, placebo-controlled study of extended-release niacin on atherosclerosis progression in secondary prevention patients treated with statins. Circulation 2004; 110:3512-3517
7. Rubins HB, Robins SJ, Collins D, et al. Gemfibrozil for the secondary prevention of coronary heart disease in men with low levels of high-density lipoprotein cholesterol. Veterans Affairs High-Density Lipoprotein Cholesterol Intervention Trial Study Group. N Engl J Med 1999; 341:410-418
8. Nissen SE, Tsunoda T, Tuzcu EM, et al. Effect of recombinant ApoA-I Milano on coronary atherosclerosis in patients with acute coronary syndromes: A randomized controlled trial. JAMA 2003; 290:2292-2300
9. Ansell BJ, Navab M, Hama S, Kamranpour N. et al. Inflammatory-antiinflammatory properties of high-density lipoprotein distinguish patients from control subjects better than high-density lipoprotein cholesterol levels and are favorably affected by simvastatin treatment. Circulation 2003;108:2751-2756
10. Matsuura F, Wang N, Chen W, et al. HDL from CETP-deficient subjects shows enhanced ability to promote cholesterol efflux from macrophages in an apoE- and ABCG1-dependent pathway. J Clin Invest 2006; 116:1435-1442
11. Mahley R W, Huang Y, and Weisgraber KH. Putting cholesterol in its place: apoE and reverse cholesterol transport. J Clin Invest 2006; 116: 1226-1229
Caracas, 10 de Diciembre de 2006
Gráfico 1
¿POR QUÉ ELEVAR EL COLESTEROL HDL?
Los grandes ensayos clínicos, que evaluaron la disminución del colesterol LDL, demostraron que cuanto más bajo fuese daba mejores resultados en el control de la morbilidad y la mortalidad de los pacientes con enfermedad vascular aterosclerótica. El estudio REVERSAL demostró detención de la progresión de la aterosclerosis pero no se llegó hasta la regresión (2). Los niveles obtenidos hasta bajar de 70 mg/dl fueron el resultado de la elevación de las dosis de estatinas, lo cual ha conducido hasta una reducción del 35% de los eventos cardiovasculares, pero aún queda un porcentaje muy importante de personas en riesgo de enfermedad, por lo cual el próximo enfoque fue el de elevar el colesterol HDL, que para el momento había sido relegado a un segundo plano. El control
de varios factores de riesgo simultáneos debe ser muy seriamente tomado en cuenta, sobre todo porque se avecina un incremento de la incidencia de enfermedad vascular en los próximos 15 años, a consecuencia de las actuales epidemias de obesidad y diabetes, realimentadas entre sí. Hay que eliminar el tabaquismo, controlar la dieta e incentivar el ejercicio para controlar el auge de la obesidad, regular y controlar con fuerza la hipertensión, mantener los niveles de control de LDL-C pero insistir también en la elevación del HDL-C. El promedio de HDL como valor mínimo aceptado actualmente es de 45 mg/dl para el hombre y de 55 mg/dl para la mujer. Niveles superiores a 60 mg/dl se consideran buenos y existe una relación de que por cada 1 mg/dl de incremento de HDL-C hay una reducción entre el 2 % y el 3% de la incidencia de enfermedad coronaria.
FUNCIONES DEL COLESTEROL HDL
Los beneficios del HDL-C parecen deberse al transporte reverso del colesterol desde las paredes arteriales hacia el hígado, donde se prepara su excreción. Pero además, se han descubierto propiedades anti-inflamatorias, antioxidantes, antitrombóticas e inductoras de óxido nítrico. La presencia de estas propiedades no han podido demostrar beneficios in vivo en grandes poblaciones, a las cuales se les pudiera elevar el HDL-C. De las pocas situaciones clínicas evaluadas, una de las más prometedoras es la del ApoA-1 Milano. Esta es una variante poco usual del principal constituyente del HDL-C, fue descubierta por los Dres. Cesare Sirtori y Guido Francheschini, de la Universidad de Milan, en Italia, en un grupo de italianos, parientes entre sí, con valores de HDL-C bajos pero sin enfermedad cardiovascular (3). Posteriormente el Dr. Prediman Shah, en Los Angeles, indujo regresión de la aterosclerosis en modelos animales después de inyectar ApoA-1 Milano (4). Más recientemente el Dr. Nissen, realizó la aplicación en humanos, como describiré más adelante.
¿COMO SUBIR EL COLESTEROL HDL?
Hay demostración de elevación del HDL-C mediante cambios en el estilo de vida como realizar ejercicio regularmente, dejar de fumar, perder peso y hacer dieta adecuada, e incluso beber alcohol moderadamente. La elevación de HDL-C a través de estos efectos no farmacológicos es modesta. A continuación, a manera de gráficos coloco en forma esquemática los efectos mencionados sobre el HDL (gráficos 2 al 8)
 Las estatinas disminuyen los niveles de lipoproteína de baja densidad (LDL) colesterol y proteína C reactiva (PCR). Se evaluaron las relaciones entre el colesterol LDL y los niveles de PCR logrado después del tratamiento con 80 mg de atorvastatina o 40 mg de pravastatina por día y el riesgo de recurrencia infarto de miocardio o muerte por causas coronarias entre 3745 pacientes con síndromes coronarios agudos. Los pacientes en quienes el tratamiento con estatinas dado a los niveles de colesterol LDL inferior a 70 mg por
Las estatinas disminuyen los niveles de lipoproteína de baja densidad (LDL) colesterol y proteína C reactiva (PCR). Se evaluaron las relaciones entre el colesterol LDL y los niveles de PCR logrado después del tratamiento con 80 mg de atorvastatina o 40 mg de pravastatina por día y el riesgo de recurrencia infarto de miocardio o muerte por causas coronarias entre 3745 pacientes con síndromes coronarios agudos. Los pacientes en quienes el tratamiento con estatinas dado a los niveles de colesterol LDL inferior a 70 mg por